背景介绍
BACKGROUND
氨探生物始终以高水平、高标准、高投入为标准,致力于建立一个高质量的自建代谢物标准品数据库,并且一直在改变、在完善,持续推进代谢物鉴定的覆盖度和准确度。
近年来,肠道微生物结构及其代谢物谱与宿主代谢之间的相互作用已经在各种动物模型和人群中展开研究,实验数据表明,肠道微生物相关代谢物不仅对肠道健康,而且对身体里的许多其他系统(包括大脑)都有巨大的影响;肠道微生物生态失衡与许多疾病的发生具有密切的相关性,如肠易激综合征、肿瘤、肾衰竭、神经类疾病、肥胖与糖尿病等,肠道微生物代谢物作为互补的宿主受体成为关键信号分子会产生重要影响,利用微生物代谢组学可以监测这些“信号分子”的变化及影响。
综合调研相关领域文献发现将近300多种常见的微生物-宿主代谢相关产物,包括胆汁酸、短链脂肪酸、氨基酸、苯甲酰和苯基衍生物、吲哚衍生物、脂类、胆碱、酚类、脂类、维生素、激素类以及多胺类等,其在宿主中扮演着重要的角色。但是,大部分文献研究仅针对于某一类代谢物进行靶向定量方法开发,这种模式就会造成成本的增大,如必须购买关注的代谢物的高纯度标准品和同位素重标,同时也会造成检测通量低、覆盖深度低的状况。
非靶向代谢组学作为一种相对全面、连续动态、无刺激的分析手段,能够全面的、深度的收集代谢组数据;结合高通量数据库检索等功能就可以实现快速、准确地对大量代谢物质进行鉴定和注释,解决通量及深度问题;而建立适用肠道微生物相关代谢物的鉴定及注释的质谱数据库,用于定性定量鉴定及确证,将解决耗费财力的购买标准品的问题。
基于此,氨探生物独立开发建立并经过严格验证的肠道微生物代谢数据库(专利公开号:CN115083528B;HK40075007A1),基于高分辨质谱检测技术,共同为肠道微生物代谢组学研究提供有效技术支撑和高度的可重复性和可靠性。可实现,在不同时检测代谢物标准品的情况下,快速、高通量的定性及定量检测数据库中已包含405种肠道微生物相关代谢物(图1),大大提高了检测速度和效率。
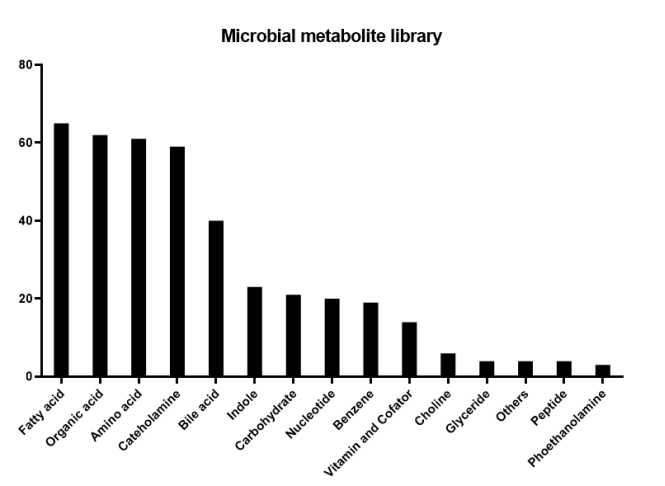
图1 肠道微生物代谢物数据库中代谢物分类
肠道微生物代谢物数据库构建全流程
Step 1-标准品数据库构建流程:
1.1 根据目前国际上认可的且应用广泛的代谢物公共数据库(如HMDB、KEGG、SMPDB及METLIN等)选取目前已经有文献报道、且在生物样本(血、尿、组织等)中已经被定性且定量检测到的肠道微生物相关代谢物作为候选目标代谢物购买相对应的高纯度标准品;
1.2 根据标准品极性的不同确定标准品的最佳稀释溶剂(甲醇、异丙醇、DMSO等)配制标准品溶液,并将配置好的标准品溶液于-80℃条件下保存,用于构建数据库的标准品溶液浓度控制在2-5mg/ml即可;
1.3 将肠道微生物相关代谢物标准品的稀释液经高分辨质谱联用仪,分别在正离子和负离子模式下,优化质谱采集方法,实现一次进样同时完成6种不同能量10、20、30、40、50、60eV的CE碰撞能量下产生一级和二级谱图的采集,确保不同性质的标准品均被成功建库,使得化合物的碎片和谱图库更为完整和丰富;
1.4 将肠道微生物相关代谢物的标准品混合溶液经C18和HILIC分离体系进行超高效液相色谱洗脱检测,获取肠道微生物相关代谢物的保留时间,并录入质谱数据库,完成标准品的构建流程。
· Step 2-数据库验证流程:
2.1 标准品数据库原始文件与新建数据库的匹配其实相当于一种“自证”的过程,源于标准品原始文件的数据库,再去对标准品进行注释,可以检查建库过程中原始文件和谱图导入有无失误,其次可以检查数据库的质量;
2.2 基于不同类型生物样本的数据库验证流程,是对每次更新的标准品数据库的最终考量。数据库最终是服务于项目的,不同类型生物样本代谢物鉴定数量的稳定提升才是数据库不断更新的最终目标。
· Step 3-数据库注释流程:
3.1 根据目前国际上认可的且应用广泛的代谢物公共数据库(如HMDB、KEGG、SMPDB及METLIN等)对这些肠道微生物相关代谢物进行通路注释;
3.2 全面的收集、整理肠道微生物相关代谢物的信息包括中文名称、英文名称、分子式、CAS号、代谢物生物类别、代谢物类别亚类、mol文件、HMDB ID、KEGG ID、ChemSpider ID、Pubchem ID、SMILES、Description等,将上述信息录入mzvault建库系统中新建的质谱数据库,对验证后的质谱数据库进行全面人工注释。
经上述3个流程(图2),最终构建得到了经过严格验证的405种肠道微生物相关代谢物注释质谱数据库;该数据库还支持多种格式导出如.txt、.msp、.db、.csv等,适用于多种代谢组学分析软件基于本谱图库进行比对;本数据库也将开发html网页格式,用于代谢物快速查找。
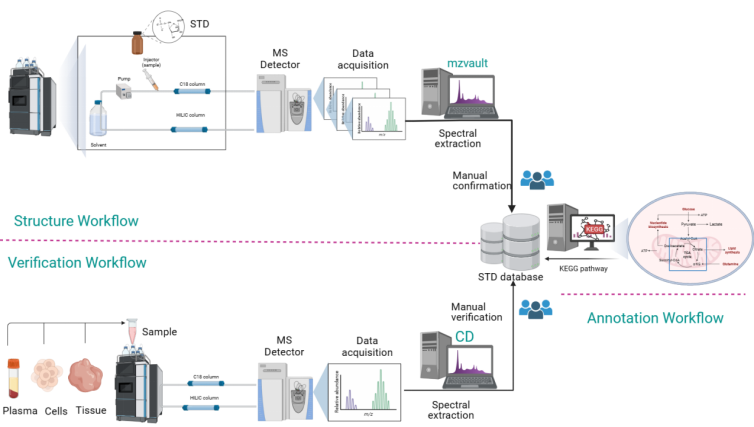
图2 肠道微生物相关代谢物质谱数据库建立、验证及注释标准流程
血浆样品分析
基于肠道微生物代谢产物数据库,采用非靶向代谢组学的检测方法,实现血浆样品中肠道微生物代谢物的检测(图3)。
· 样品制备:基于自动化AOSP-Elite 1000的前处理流程(适用于多种生物样品),同时加入10余种同位素内标进行灵敏度的监测和绝对定量分析;同时在前处理过程中对样本进行随机化处理,降低样本制备环节误差。
· LC-MS分析:为了获得更多的代谢产物鉴定结果,采用HILIC和C18两种色谱进行分离;质谱检测中,使用高灵敏度和快扫描速度的Q Exactive Plus超高分辨质谱和两种分离体系进行高覆盖的检测。为了确保检测结果的稳定性,每6-10个样品间设置1个QC用于数据质控。
· 数据处理:采用Compound Discoverer软件进行数据库匹配检索和定量,可以深度和准确获取肠道微生物相关代谢物鉴定结果。
· 统计分析:采用氨探生物自主研发的数据统计分析云平台OMIA,可实现一站式组学数据质控(OBC)和差异分析(ODE)、多组学联合分析(OIA)以及机器学习模型(OML)的构建。
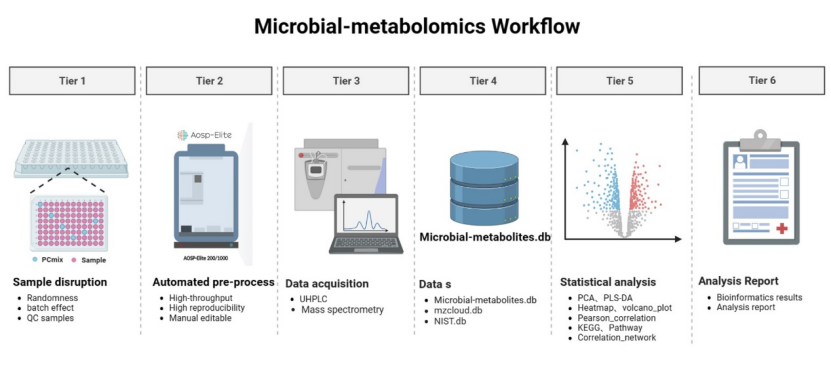
图3 血浆样品中肠道微生物代谢物检测流程
如果您对《肠道微生物相关代谢物高通量筛查质谱数据库》感兴趣,或者有宝贵的意见和建议,请联系我们:info@untangledbio.com。
参考文献
Untangled Biosciences
解构健康奥秘、探寻生命答案,氨探生物以一流的分子表型组平台和成熟的临床转化应用体系,为优秀的研究团队进行技术和数据赋能,致力于实现分子表型水平的精准诊疗。




